利用两对近等基因系(NILs)CCRI12和CSSL1接种大丽轮枝菌(Verticillium dahliae),以评估色素腺体对黄萎病抗性的功能(图1a)。在接种的近等基因系的叶片和茎中测定了三个具有代表性的腺体形成基因CGF2、CGF3和GRAS1的转录水平,这三个基因分别控制腺体密度、全株腺体形成和茎腺体形成。在这两对品系中,与有腺体棉花(CCRI12/CSSL1-GL)相比,无腺体棉花(CCRI12/CSSL1-gl)叶片和茎中CGF2和CGF3的表达水平均显著下调(图1b、c)。然而,在相同的比较中,GRAS1的下调幅度低于CGF2和CGF3,且CCRI12-gl品系叶片中GRAS1的表达水平与CCRI12-GL品系相比无显著变化(图1d)。与腺体表型一致的是,接种V.dahliae后,有腺体品系CCRI12/CSSL1-GL的病害症状减轻,病情指数降低,棉酚含量增加,而无腺体品系CCRI12/CSSL1-gl则相反(图1e-g)。CCRI12/CSSL1-gl植株叶片和茎中五个棉酚生物合成基因CDNC、CYP706B1、DH1、CYP82D113和CYP71BE79的转录水平均显著低于CCRI12/CSSL1-GL植株,仅有个别例外。接种V.dahliae(1×107 spores/mL)三天后,CCRI12近等基因系和CSSL1近等基因系中,有腺体植株根部这些棉酚生物合成基因的转录水平较无腺体植株显著上调(图1h)。
通过沉默GbCDNC和GbCYP706B1评估棉酚对棉花黄萎病抗性的影响。与空载体对照TRV:00植株相比,TRV:GbCDNC和TRV:GbCYP706B1植株中这些基因的表达水平显著下调。接种V.dahliae后,TRV:GbCDNC和TRV:GbCYP706B1棉花幼苗的病害症状更严重,病情指数更高,与相应的TRV:00植株相比。此外,TRV:GbCDNC和TRV:GbCYP706B1棉花幼苗根部的棉酚含量较TRV:00棉花幼苗显著降低。这些结果表明,有腺体棉花品系对V.dahliae感染的抗性高于无腺体品系,这可能是通过有腺体品系中CGF基因CGF2/3和GRAS1以及棉酚生物合成基因的高表达实现的。
图1.中国农业科学院棉花研究所选育的12号(CCRI12)棉花无腺体近等基因系(NILs)及染色体片段代换系1号(CSSL1)相较于其对应的有腺体姊妹系,对黄萎病的抗性有所降低。(a)有腺体品种CCRI12-GL(或CSSL1-GL)与无腺体品种CCRI12-gl(或CSSL1-gl)的叶片和茎的腺体特征。(b-d)CCRI12和CSSL1植株叶片和茎中棉花腺体形成(CGF)基因CGF2、CGF3和GRAS1的相对转录水平。(e、f)接种V.dahliae后21天,CCRI12和CSSL1植株的病害症状(e)和病情指数(f)。(g)接种V.dahliae后0天或3天,CCRI12和CSSL1植株根部的棉酚含量。(h)接种V.dahliae后3天,CCRI12和CSSL1植株根部棉酚生物合成基因的相对转录水平。数据为三次生物学重复的平均值±标准差(n=3;每个生物学重复包含三株独立植株)。星号表示经Student's t检验确定的统计学显著差异:*,P<0.05;**,P<0.01;***,P<0.001。dpi,接种后天数。
敲低CGF基因GbCGF2/3会降低对黄萎病菌(Verticillium dahliae)的抗性
利用病毒诱导基因沉默(VIGS)方法,以抗病品种海岛棉Hai7124为材料,阐明了棉花腺体形成(CGF)基因GRAS1和CGF2/3在黄萎病抗性中的功能。将GbGRAS1和GbCGF2/3与分别来自澳洲棉(G.australe)和陆地棉(G.hirsutum)的原始克隆序列进行氨基酸比对,结果显示GauGRAS1与GbGRAS1的相似度为88.67%,GhCGF2与GbCGF2之间仅有一个氨基酸差异,而GhCGF3与GbCGF3的序列完全相同。对棉花植株不同器官中腺体形成基因的表达模式进行分析,结果显示GbGRAS1在茎和叶中的转录水平显著高于根,而GbCGF2和GbCGF3在根、茎和叶中的表达较为均匀。接种黄萎病菌(V.dahliae)后,作为抵御土传病原体的第一道防线,根中GbCGF2和GbCGF3的表达水平分别在6小时和12小时后开始上升,于24小时达到峰值(增加4倍),随后在72小时恢复至正常或接近正常水平(图2a)。然而,在整个过程中,GbGRAS1的转录水平保持不变(图2a)。在海岛棉Hai7124中,通过VIGS沉默GbGRAS1、GbCGF2和GbCGF3后,与各自的对照TRV:00植株相比,其转录水平降低了6倍以上(图2b-d)。在TRV:GbGRAS1、TRV:GbCGF2和TRV:GbCGF3棉花植株中,分别观察到了预期的三个腺体性状变化:茎腺体消失、全株腺体密度降低和全株腺体丧失(图2e)。作为监测VIGS效率的标记,GbCLA基因也被沉默,TRV:GbCLA植株新长出的真叶出现白化表型,表明VIGS系统正常工作(图2f)。接种V.dahliae后,与对照TRV:00植株相比,TRV:GbCGF2和TRV:GbCGF3植株表现出更严重的萎蔫、黄化和落叶,病情指数值更高(图2g,h)。此外,与TRV:00植株相比,TRV:GbCGF2和TRV:GbCGF3棉花植株茎部维管组织中的棕色染色程度更深,且在PDA平板上从感染茎部生长出的V.dahliae更多(图2i)。与对照TRV:00植株相比,TRV:GbGRAS1、TRV:GbCGF2和TRV:GbCGF3棉花植株根部棉酚生物合成基因CDNC、CYP706B1、DH1、CYP82D113和CYP71BE79的表达均下调。与TRV:00植株相比,TRV:GbCGF2和TRV:GbCGF3植株茎和叶中的棉酚含量也有所降低(图2j)。然而,TRV:GbGRAS1植株仅在茎中棉酚含量降低,叶中棉酚含量未受影响(图2j)。这些结果表明,沉默棉花植株中的GbCGF2或GbCGF3基因会降低其对棉花黄萎病的抗性。

图2.沉默棉花腺体形成(CGF)基因GbCGF2和GbCGF3降低了棉花对黄萎病菌(Verticillium dahliae)的抗性。(a)海岛棉品种Hai7124接种V.dahliae后,GbGRAS1、GbCGF2和GbCGF3的表达模式。(b-d)分别沉默GbGRAS1(TRV:GbGRAS1)、GbCGF2(TRV:GbCGF2)和GbCGF3(TRV:GbCGF3)的棉花植株中,GbGRAS1、GbCGF2和GbCGF3的相对转录水平。(e)TRV:GbGRAS1、TRV:GbCGF2和TRV:GbCGF3棉花植株叶片和茎中的腺体性状。(f)接种TRV:GbCLA载体14天后棉花植株的白化表型。(g)接种V.dahliae 21天后,TRV:00、TRV:GbGRAS1、TRV:GbCGF2和TRV:GbCGF3幼苗的发病症状。(h,i)图中所示TRV:00、TRV:GbGRAS1、TRV:GbCGF2和TRV:GbCGF3棉花植株的病情指数(h)、茎部维管染色和PDA平板上茎部真菌生长情况(i)。(j)TRV:00、TRV:GbGRAS1、TRV:GbCGF2和TRV:GbCGF3棉花植株叶片和茎中的棉酚含量。数据为三次生物学重复的平均值±标准差(n=3;三次独立植株/生物学重复)。星号表示通过Student's t检验确定的统计学显著差异:*,P<0.05;**,P<0.01;***,P<0.001。
对沉默GbCGF2/3的棉花根系进行转录组分析,以筛选与抗V.dahliae相关的下游基因
通过在接种黄萎病菌(V.dahliae)21dpi(此时观察到最显著疾病症状差异)时,利用受感染的TRV:GbCGF2或TRV:GbCGF3与TRV:00棉花植株的根部进行两组RNA-seq实验,筛选出了GbCGF2和GbCGF3下游参与抗黄萎病菌的基因。TRV:00、TRV:GbCGF2和TRV:GbCGF3棉花植株根部的基因表达水平(RPKM值)和倍数变化。在TRV:GbCGF2与TRV:00对比组中,有2558个基因上调,3708个基因下调(图3a);在TRV:GbCGF3与TRV:00对比组中,有2226个基因上调,3806个基因下调(图3b)。TRV:GbCGF2与TRV:00对比组和TRV:GbCGF3与TRV:00对比组之间共有1747个基因上调,2460个基因下调(图3c,d)。利用Metascape对这些共同的差异表达基因进行了功能基因本体(GO)富集分析。上调基因在“半胱氨酸和甲硫氨酸代谢”、“缬氨酸、亮氨酸和异亮氨酸降解”、“光合作用”、“过氧化物酶体”和“脂肪酸降解”等条目中高度富集(图3e),而下调基因则在“苯丙烷生物合成”、“黄酮类生物合成”、“苯丙氨酸代谢”、“角质、木栓质和蜡质”以及其他植物代谢过程中高度富集(图3f)。角质、木栓质和蜡质生物合成途径已知与植物免疫有关。黄萎病菌是一种引起棉花黄萎病的真菌病原体,它通过穿透根部组织侵入棉花植株。因此,由角质、木栓质和蜡质生物合成途径形成的植物物理屏障可能在黄萎病的发病过程中发挥重要作用。因此,我们选择了与“角质、木栓质和蜡质”途径相关的基因进行详细研究。参与木栓质生物合成的几个基因,GbCYP86A1、GbFAR3、GbHHT1和GbPXG4,在GbCGF2和GbCGF3沉默的植株中的表达水平均低于对照植株(图3g)。RT-qPCR测定结果显示,与对照植株相比,GbCGF2和GbCGF3沉默的植株中GbFAR3的表达水平至少下调了5倍(图3h)。这些结果共同表明,色素腺相关过程通过调节角质、木栓质和蜡质生物合成途径来增强棉花对黄萎病的抗性。

图3.对沉默GbCGF2和GbCGF3的棉花根系进行转录组分析,以深入探究其对黄萎病菌(Verticillium dahliae)抗性的分子机制。(a,b)与对照(TRV:00)植株相比,沉默GbCGF2(a)和GbCGF3(b)的棉花植株中差异表达基因(DEGs)的数量。红色柱状图表示上调的DEGs,蓝色柱状图表示下调的DEGs。(c,d)各比较组间DEGs的维恩图。数字表示各组间共有和特有的DEGs数量。(e,f)利用KEGG通路分析,对维恩图中上调(e,1747个基因)和下调(f,2640个基因)的基因进行富集分析。x轴表示KEGG条目映射的总DEGs与所有基因的比例,颜色条表示基因的累积超几何P值,气泡表示KEGG条目中的基因数量。(g)从RNA-seq数据中获得的与角质、木栓质和蜡质生物合成相关基因的表达水平。颜色条表示(log2(RPKM))表达水平的增加(红色)和减少(蓝色),|fold-change|>2。(h)通过逆转录-定量聚合酶链反应测定的GbCGF2和GbCGF3沉默棉花植株根部下调基因的相对表达水平。数据为三个生物重复的平均值±标准差(n=3;三个独立植株/生物重复)。星号表示通过Student's t-检验确定的统计学显著差异:*,P<0.05;**,P<0.01。
下调或敲除木栓质生物合成基因GbFAR3.1会降低棉花对黄萎病菌的抗性
对GbFAR基因的系统发育分析显示,在G.barbadense中存在五个家族:GbFAR1、GbFAR2、GbFAR3、GbFAR5和GbFAR10,且每个家族中同源基因的拷贝数差异显著:GbFAR5和GbFAR10各含一个拷贝,GbFAR1和GbFAR2各含两个拷贝,而GbFAR3则含有四个拷贝。GbFAR3的四个同源基因(GbFAR3.1-A、GbFAR3.1-D、GbFAR3.2-A和GbFAR3.2-D)的序列及保守基序高度相似。对这些GbFAR同源基因的结构(外显子/内含子)分析显示,A基因组和D基因组同源基因的外显子分布极为相似,表明这些GbFAR基因具有平行功能。对黄萎病菌处理后这些木栓质生物合成基因转录水平的时间进程分析显示,GbFAR3.1和GbFAR3.2的表达在多个时间点显著上调,而GbFAR1、GbFAR2和GbFAR5的表达在此期间无显著变化(图4a)。值得注意的是,GbFAR3.1的表达模式与GbCGF2和GbCGF3高度相似(图2a),均从接种后6小时开始上升,24天时达到峰值(增加8倍),随后逐渐下降(图4a)。单独沉默GbFAR1、GbFAR2、GbFAR3.1、GbFAR3.2或GbFAR5后,接种黄萎病菌的棉花植株中,仅在TRV:GbFAR3.1、TRV:GbFAR3.2和TRV:GbFAR5植株中观察到病情加重、病情指数升高、维管束棕色染色加深以及感染茎部黄萎病菌生长增多,而TRV:GbFAR1和TRV:GbFAR2植株与对照植株相比无显著差异。TRV:GbFAR3.1植株的病情症状和病情指数均高于TRV:GbFAR3.2棉花植株。进一步地,我们单独下调和敲除了GbFAR3.1以探究其在黄萎病菌感染过程中的功能。与TRV:00植株相比,GbFAR3.1沉默植株中GbFAR3.1的表达降低,显著降低了对黄萎病菌的抗性,病情指数更高(图4b-e)。与TRV:00植株相比,TRV:GbFAR3.1植株的茎部棕色条纹更多,茎部黄萎病菌生长更多,维管组织中的真菌生物量增加了约2倍(图4f,g)。与对应的野生型(WT)植株相比,再生转基因GhFAR3.1-Cas9突变体植株的T1代也表现出降低的黄萎病抗性,病情指数更高。
利用标记了绿色荧光蛋白(GFP)的黄萎病菌进行感染实验,以可视化棉花根系的感染过程。与TRV:00植株相比,TRV:GbFAR3.1植株中观察到的绿色荧光强度更高,黄萎病菌孢子数量更多,且接种黄萎病菌后3、5和7天时,TRV:GbFAR3.1植株根系中的相对真菌生物量积累也更多。
通过浸润携带GFP标记的GbFAR3.1表达载体的烟草叶片,确定了GbFAR3.1的亚细胞定位(图4h)。检测到GbFAR3.1蛋白位于内质网(ER)中(图4i),这与它在木栓质生物合成途径中的功能一致。与TRV:00植株相比,TRV:GbFAR3.1植株中木栓质组成单体脂肪酸C16-C24的含量显著降低(图4j)。在GbFAR3.2沉默植株中也观察到类似结果,C18-C24脂肪酸含量降低,表明这两个同源基因具有平行功能。与TRV:00植株相比,TRV:GbFAR3.1植株根系中木栓质生物合成基因GbLACS1、GbKCS1/2、GbGAPT5和GbCYP86A1(但不包括GbCYP86A2)的转录水平显著降低。与GbFAR3.1沉默植株中角质、木栓质和蜡质形成所需的长链脂肪醇生物合成受到抑制相一致,这些植株的根细胞壁变得非常薄,且片层结构消失(图4k)。总体而言,这些结果表明,GbFAR3.1参与棉花根系细胞壁中木栓质的生物合成,并通过在根细胞壁中形成木栓质保护层来提高棉花对黄萎病菌的抗性。
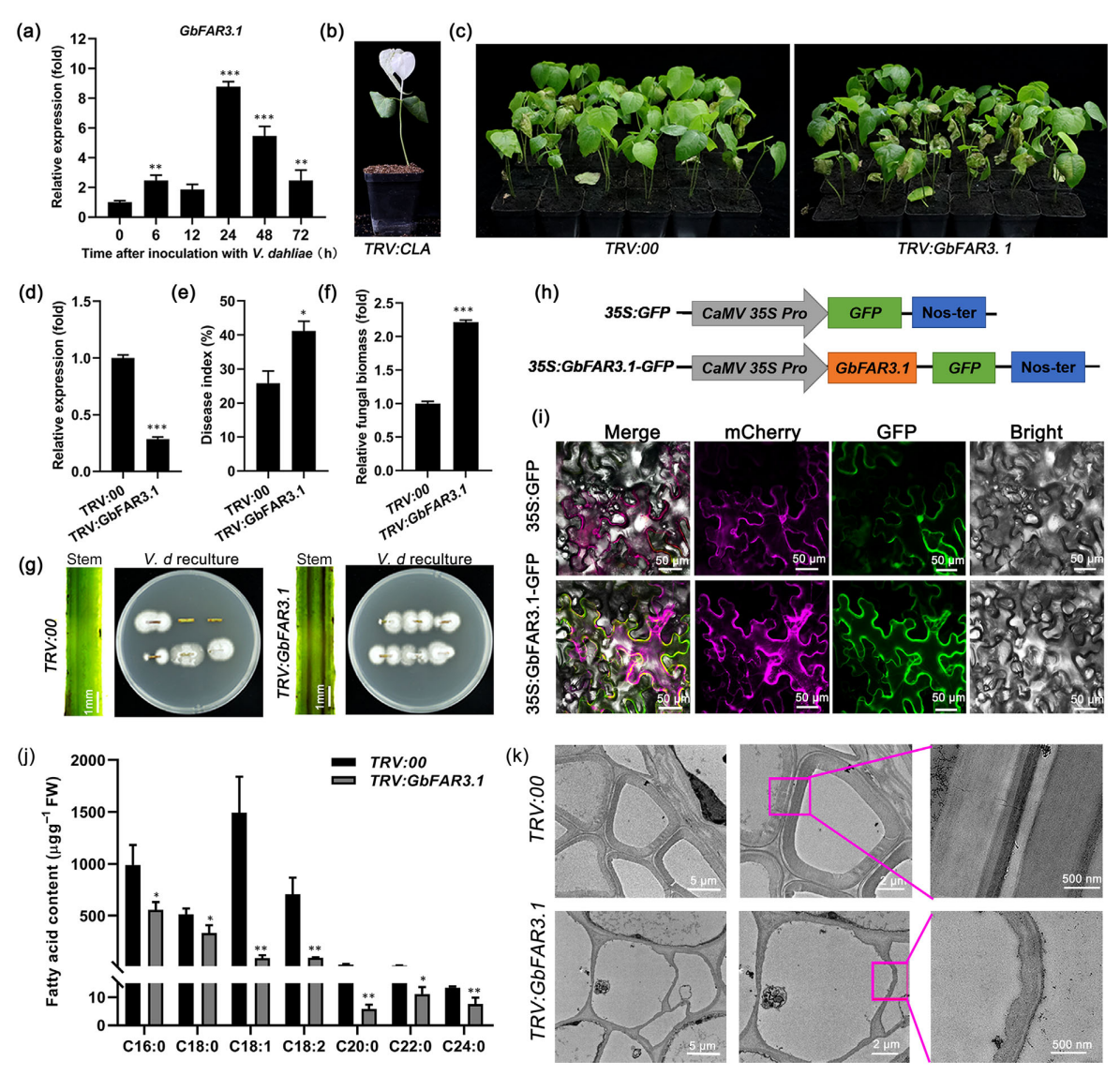
图4.下调脂肪酸酰基辅酶A还原酶3.1(GbFAR3.1)降低棉花对黄萎病菌(Verticillium dahliae)的抗性。(a)感染黄萎病菌(V.dahliae)的海岛棉品种Hai7124中GbFAR3.1的表达模式。(b)接种TRV:GbCLA载体14天后棉花植株的白化表型。(c)接种黄萎病菌(V.dahliae)21天后TRV:00和TRV:GbFAR3.1幼苗的病情症状。(d)GbFAR3.1沉默(TRV:GbFAR3.1)棉花植株中GbFAR3.1的表达。(e-g)中所示TRV:00和TRV:GbFAR3.1棉花植株的病情指数(e)、茎部真菌生物量(f)、茎部维管束染色及PDA平板上茎部真菌生长情况(g)。(h)GbFAR3.1-GFP报告基因模型示意图。(i)本氏烟草叶片中GbFAR3.1-GFP的亚细胞定位。Mcherry代表带有HDEL:DsRed(红色)载体的内质网(ER)标记。(j)TRV:00和TRV:GbFAR3.1幼苗根系中木栓质单体脂肪酸组成。(k)使用透射电子显微镜观察TRV:GbFAR3.1和TRV:00棉花植株的根细胞壁。数据为三次生物学重复的平均值±标准差(n=3;三次独立植株/生物学重复)。星号表示通过Student’s t检验确定的显著差异:*,P<0.05;**,P<0.01;***,P<0.001。dpi,接种后天数。
GbCGF2/3通过结合其启动子正向调控GbFAR3.1的表达
转录组学分析以及GbCGF2(NAC)和GbCGF3(bHLH)的转录因子特性,我们推测这两个基因是否能够直接激活GbFAR3.1的转录。通过使用融合了绿色荧光蛋白(GFP)的GbCGF2和GbCGF3表达载体,在烟草(N.benthamiana)叶片中进行瞬时表达实验的亚细胞定位分析显示,绿色荧光信号与用DAPI染色的细胞核共定位,这表明GbCGF2和GbCGF3被定位到细胞核中,可能进行转录活动。在酵母中,使用将GbCGF2或GbCGF3的编码序列(CDS)融合到GAL4 DNA结合域的载体进行的转录激活实验显示,只有GbCGF2能够转录激活报告基因GAL4,而GbCGF3则不能,这表明GbCGF2具有转录激活功能,而GbCGF3在该实验中没有表现出此功能。
对GbFAR3.1、GbCGF2和GbCGF3基因上游2-kb启动子区域中存在的顺式作用调控元件的分析揭示了许多E-box(CANNTG)顺式元件的存在,这些元件是bHLH和NAC识别位点,表明它们的表达可能受到bHLH家族转录因子的调控。为了测试GbCGF2和GbCGF3是否能够结合到GbFAR3.1基因的启动子区域,我们进行了酵母单杂交(Y1H)实验。pAbAi-proGbFAR3.1的自激活实验显示,仅含有报告构建体的Y1H Gold报告菌株在SD/-Ura + 700 ng/ml AbA培养基上生长受到抑制。随后,将pAbAi-proGbFAR3.1酵母报告菌株用pGADT7-GbCGF2或pGADT7-GbCGF3效应子质粒转化,结果得到的转化子能够在SD/-Ura+700ng/ml AbA培养基上生长,这表明GbCGF2或GbCGF3能够有效地结合到GbFAR3.1的启动子上(图5b)。进一步,我们使用由GbFAR3.1启动子驱动的LUC报告构建体(ProGbFAR3.1:LUC)进行了LUC成像分析,并通过农杆菌(Agrobacterium tumefaciens)浸润法将该构建体与35S:GbCGF2或35S:GbCGF3效应子共浸润到烟草叶片中。与用ProGbFAR3.1:LUC和对照空载体(EV)共转化的叶片相比,用ProGbFAR3.1:LUC和35S:GbCGF2或35S:GbCGF3共转化的叶片中LUC荧光强度增加(图5c,d)。与对照EV相比,当由GbFAR3.1突变启动子驱动并与GbCGF2和GbCGF3共表达时,LUC基因的LUC荧光强度显著降低(图5e-g)。此外,通过电泳迁移率变动分析(EMSA)证明了GbCGF2或GbCGF3与GbFAR3.1启动子上预测的E-box结合位点的结合(图5h,i)。这些结果表明,GbCGF2和GbCGF3在棉花中作为GbFAR3.1表达的转录激活因子发挥作用。

图5. GbCGF2/3调控GbFAR3.1的表达。(a)pAbAi-proGbFAR3.1的自激活实验。仅含有pAbAi-proGbFAR3.1报告构建体的Y1HGold报告菌株在SD(合成缺失)/-Ura+700ng/ml AbA(金担子素A)培养基上生长受到抑制。(b)在酵母单杂交(Y1H)实验中,GbCGF2或GbCGF3与GbFAR3.1的启动子结合。用pGADT7-GbCGF2/-GbCGF3和pAbAi-proGbFAR3.1质粒转化的Y1H Gold报告菌株能够在SD/-Ura + 700 ng/ml AbA培养基上生长。(c,d)使用GbFAR3.1或GbFAR3.1突变启动子与GbCGF2或GbCGF3相互作用的荧光素酶(LUC)成像分析。(e)示意图显示GbCGF2/GbCGF3在LUC和电泳迁移率变动分析(EMSA)中与GbFAR3.1启动子的E-box基序结合。野生型基序(5’-CACGTG-3’)和突变序列(5’-AAAAAA-3’)以品红色字体显示。(f,g)LUC活性显示为荧光强度的倍数变化。LUC信号在浸润后2天收集,误差条表示每次三个重复结果(每次三片叶子)的平均值±标准差(n≥3,P<0.05;**,P<0.001,t检验)。(h,i)在EMSA实验中,GbCGF2/GbCGF3直接与GbFAR3.1启动子的E-box基序结合。生物素标记的野生型(WT)探针和突变探针单独或与纯化的重组GbCGF2-His和GbCGF3-His一起孵育。加入竞争探针(109、509和1009)以确定结合的特异性。
CRISPR/Cas9介导的CGF2/3敲除通过减少木栓质积累削弱棉花对V.dahliae的抗性
在有腺体的陆地棉品系“jin668”中,通过CRISPR/Cas9技术敲除了GhCGF2或GhCGF3。为确保基因突变的效率,设计了两个sgRNA,每个sgRNA分别针对GhCGF2和GhCGF3的CDS区域,构建于sgRNA-Cas9表达盒中(图6a)。成功再生的T0代转基因GhCGF2-Cas9-19和GhCGF3-Cas9-5突变体植株分别表现出腺体密度降低和全株腺体缺失的表型(图6b)。从GhCGF2-Cas9-19和GhCGF3-Cas9-5植株的基因组DNA中扩增出Cas9基因(扩增片段为827bp),证实了突变体中存在Cas9-sgRNA表达盒(图6c)。同时,扩增出含有GbU6-7启动子和sgRNA1/sgRNA2-GhCGF2或sgRNA1/sgRNA2-GhCGF3两个靶点(扩增片段为500bp)的载体骨架,也证明了基因编辑表达盒在转基因植株中正常工作所需的引导RNA的存在(图6c)。对扩增片段的测序进一步显示,GhCGF2-Cas9-19和GhCGF3-Cas9-5转基因幼苗的突变类型主要包括两个靶点之间的碱基缺失和插入(图6d)。
我们进行了V.dahliae侵染实验,以评估GhCGF2-Cas9-19和GhCGF3-Cas9-5 T1代突变体植株对黄萎病的抗性。与野生型(WT)植株相比,突变体植株在感染后表现出更严重的病害症状、更强的茎部维管褐变程度以及更大的茎部真菌生长量,当感染茎段置于PDA培养基上培养时,这表明突变体对V.dahliae感染的抗性显著降低(图6e)。此外,与WT植株相比,GhCGF2-Cas9-19和GhCGF3-Cas9-5突变体植株的病情指数值分别增加了约20%和30%(图6f)。透射电子显微镜观察显示,GhCGF2-Cas9-19和GhCGF3-Cas9-5突变体植株的根细胞壁厚度显著降低,且片层结构消失,表明木栓质的沉积受到抑制(图6g)。与WT植株相比,GhCGF2-Cas9-19和GhCGF3-Cas9-5突变体植株中GhFAR3.1的转录水平分别降低了2倍和3倍(图6h)。与WT植株相比,GhCGF2-Cas9-19和GhCGF3-Cas9-5突变体棉花植株中其他几个木栓质生物合成基因如GhKCS1/2、GhLACS1和GhCYP86A1的表达也下调,但GhCGF2-Cas9-19植株中的GhCYP86A2除外(图6h)。此外,GhCGF2-Cas9-19和GhCGF3-Cas9-5突变体植株中木栓质组成单体脂肪酸C18-C22的含量也显著低于WT植株。与WT植株相比,GhCGF2-Cas9-19和GhCGF3-Cas9-5棉花植株中棉酚生物合成基因CDNC、CYP706B1、DH1、CYP82D113和CYP71BE79的转录水平也显著下调。
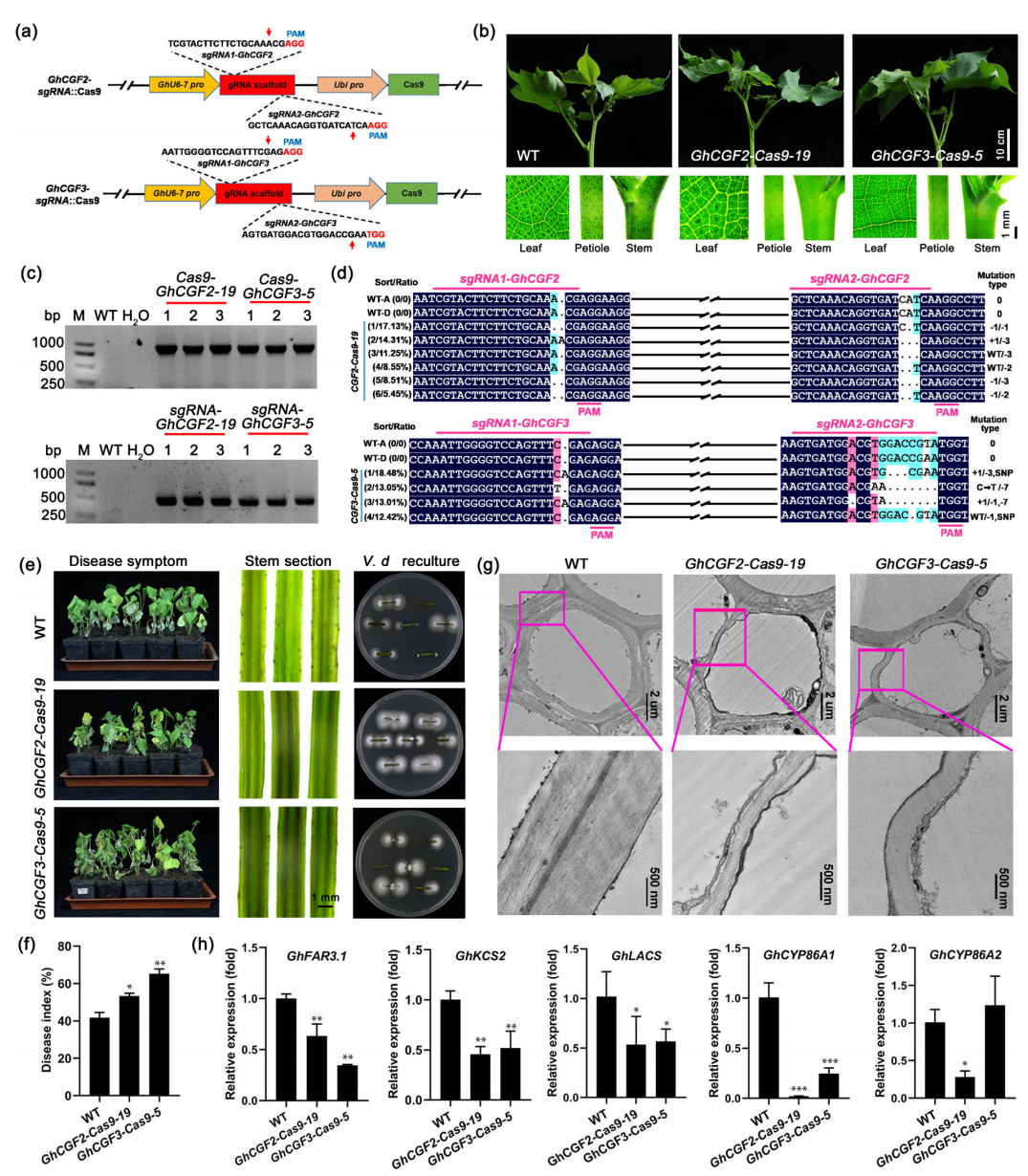
图6. CRISPR/Cas9介导的GhCGF2和GhCGF3转基因棉花植株基因编辑突变体的黄萎病抗性降低。(a)含sgRNA1/2-GhCGF2和sgRNA1/2-GhCGF3靶位点的转化载体示意图。sgRNA被设计为靶向GhCGF2或GhCGF3的A和D同源基因。(b)代表性GhCGF2-Cas9-19和GhCGF3-Cas9-5转基因T0代棉花植株叶片、叶柄和茎的腺体特征。(c)通过PCR扩增从含有Cas9和sgRNA1/2-GhCGF2或sgRNA1/2-GhCGF3表达盒的转基因棉花植株中提取的基因组DNA样品,检测Cas9基因及sgRNA-GhCGF2和sgRNA-GhCGF3靶向突变。(d)对本研究中使用的野生型(WT)、GhCGF2-Cas9-19和GhCGF3-Cas9-5植株的含靶位点基因组区域进行PCR产物测序。靶序列用品红色下划线标出。GhCGF2-Cas9-19和GhCGF3-Cas9-5植株的突变类型及突变比例显示在左侧,突变类型显示在右侧,缺失用“-”表示,插入用“+”表示,缺失或插入的碱基数用数字表示。A/D,A或D亚基因组。SNP,单核苷酸多态性。(e)用V.dahliae接种21天后,GhCGF2-Cas9-19和GhCGF3-Cas9-5转基因棉花植株(T1)的病害症状、茎部维管褐变及在PDA培养基上的茎部真菌生长情况。(f)中棉花植株的病情指数。(g)GhCGF2-Cas9-19和GhCGF3-Cas9-5转基因棉花植株根组织细胞壁的透射电镜照片。(h)GhCGF2-Cas9-19和GhCGF3-Cas9-5转基因棉花植株根部木栓质生物合成基因的相对转录水平。数据为三次生物学重复的平均值±标准差(n=3;三次独立植株/生物学重复)。星号表示经Student's t检验确定的统计学显著差异:*,P<0.05;**,P<0.01;***,P<0.001。dpi,接种后天数。
植物激素茉莉酸(JA)诱导GbCGF2/3和GbFAR3.1的表达
先前研究表明,CGF3的表达受茉莉酸(JA)处理诱导,对GbCGF2/3和GbFAR3.1启动子的分析表明,其表达可能也通过启动子区域中茉莉酸响应调控元件CGTCA框受JA调控。用3μM甲基茉莉酸(MeJA)处理抗病品种Hai7124,在处理后6、8、10和12小时,GbCGF2/3和GbFAR3.1的转录水平均提高了约2-4倍。用MeJA处理棉花植株根部后,棉酚生物合成基因CDNC、CYP706B1、DH1、CYP82D113和CYP71BE79的表达也呈现上调趋势,其中CDNC和CYP706B1上调最为显著,分别提高了约8倍和4倍。
为进一步了解GbCGF2/3和GbFAR3.1在JA介导的棉花抗黄萎病菌过程中可能发挥的作用,我们检测了TRV:GbCGF2/3和TRV:GbFAR3.1棉花植株中JA信号通路基因GbLOX、GbJAZ1、GbPDF1.2和GbPR4的转录水平。与TRV:00植株相比,TRV:GbCGF2/3和TRV:GbFAR3.1植株棉花根部GbLOX、GbPDF1.2和GbPR4的转录水平显著降低,而JA信号通路抑制因子GbJAZ1的转录水平则显著升高。与野生型(WT)植株相比,GhCGF2/3-Cas9敲除棉花植株中这些基因的转录水平也呈现出类似结果。这些结果表明,棉酚生物合成和JA介导的防御相关基因可能通过GhCGF2/3的调控参与棉花对黄萎病的抗性。
图7.腺体形成基因GbCGF2和GbCGF3通过促进棉酚及角质/木栓质合成以增强棉花对大丽轮枝菌(Verticillium dahliae)抗性的作用机制假说模型。大丽轮枝菌侵染可诱导GbCGF2和GbCGF3的表达,二者结合至木栓质生物合成基因GbFAR3.1的启动子区域并激活其转录,进而促进木栓质生物合成并加固根细胞壁,最终提升对大丽轮枝菌的抗性。此外,植物激素茉莉酸(JA)可增强GbCGF2和GbCGF3的表达,诱导棉花根部棉酚防御途径并参与宿主对大丽轮枝菌的抗性。黑色箭头表示促进作用;虚线箭头表示不确定的促进作用。bHLH,碱性螺旋-环-螺旋;JA,茉莉酸。